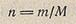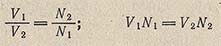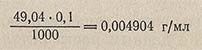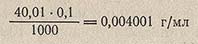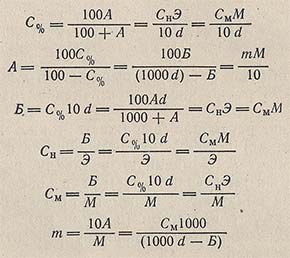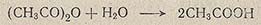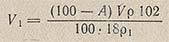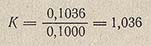- Приготовление водных растворов рецепты
- Правила выписывания
- Водные растворы
- Масляные растворы
- Спиртовые растворы
- Официнальные растворы
- Растворы для инъекций
- В ампулах
- Во флаконах
- В шприц-тюбиках
- Пример расчёта количества и концентрации раствора для выписывания рецепта.
- Приготовление растворов
- Способы выражения концентрации растворов
- Формулы перехода от одних выражений концентрации растворов к другим
- Растворимость
- Техника приготовления растворов
- Приготовление водных растворов кислот приблизительной концентрации
- Приготовление безводного раствора хлорной кислоты
- Приготовление растворов щелочей
- Приготовление водного раствора аммиака
- Приготовление рабочих растворов точной концентрации
Приготовление водных растворов рецепты
Растворы — жидкая лекарственная форма, получаемая путём растворения жидких, твёрдых или газообразных веществ в растворителе или смеси взаимосмешивающихся растворителей с образованием гомогенных дисперсных систем. Растворы являются универсальной лекарственной формой, так как их можно применять наружно, вводить минуя желудочно-кишечный тракт (парентерально) и принимать внутрь.
Несомненным преимуществом растворов является то, что действие лекарства, введенного в жидком виде, наступает быстрее, а влияние препарата бывает наиболее полным. Они могут быть официнальными и магистральными. Растворы для инъекционного применения выпускаются в ампулах и флаконах и в этом случае являются дозированными лекарственными средствами.
Растворители для растворов выбирают, исходя из свойств и природы действующего вещества или веществ, для обеспечения отсутствия возможного химическою и физико-химического взаимодействия между растворителем и действующим веществом или веществами. Растворитель не должен оказывать влияния на фармакологическую активность действующего вещества или веществ.
В качестве основного растворителя для приготовления водных растворов для внутреннего, наружного или местного применения используют воду очищенную. В неводных растворах основными растворителями являются спирт этиловый различных концентраций, масла жирные, масло вазелиновое, глицерин и др.
Воду и водные растворы, близкие по плотности к воде — отмеряют, твёрдые вещества — отвешивают. Растворители и растворы, плотность которых сильно отличается от 1,0 — отвешивают.
В общем списке растворов особняком стоят растворы для инъекций. Растворы для инъекций — жидкая лекарственная форма, предназначенная для парентерального введения. Они используются очень широко.
К лекарственным формам для парентерального применения относятся:
• инъекционные и инфузионные лекарственные формы (раствор для инъекций, эмульсия для инъекций, суспензия для инъекций, раствор для инфузий, эмульсия для инфузий);
• концентраты для приготовления инъекционных и инфузионных лекарственных форм;
• твёрдые лекарственные формы, предназначенные для приготовления инъекционных и инфузионных лекарственных форм (порошок; лиофилизат, в том числе «лиофилизнрованный порошок»);
• лекарственные формы для имплантации (имплантат, таблетка для имплантации и т.д.).
Преимуществами парентерального способа (в форме инъекций) введения лекарственных веществ являются:
• быстрота развития фармакологического эффекта;
• высокая точность дозировки;
• 100% биологическая доступность (лекарственные вещества минуют желудочно-кишечный тракт и печень);
• полностью снимаются ощущения, связанные с неприятным запахом и вкусом лекарственных препаратов;
• возможность введения пациенту в бессознательном состоянии.
Недостатки: • определенные требования, предъявляемые к лекарственным формам для инъекций;
• ввиду того что лекарственные средства вводят минуя защитные барьеры организма, возникает серьезная опасность внесения инфекции;
• при введении лекарственных средств в сосудистое русло (артерии, вены) возникает опасность эмболии вследствие попадания твердых частиц или пузырьков воздуха, если их диаметр превышает диаметр сосуда. При этом в ряде случаев возможен летальный исход;
• болезненность инъекционного метода, негативная реакция больного «на шприц и белый халат»;
• необходимость специальных инструментов: шприц, система для инфузионного вливания и др.;
• инъекционный способ требует наличия высококвалифициро-ванного медицинского персонала, особенно при внутриартериальном и внутривенном введении.
В качестве растворителей для инъекционных препаратов обычно используют: • воду для инъекций (aqua pro injectionibus);
• 5 % раствор глюкозы (solutio Glucosi 5 %);
• изотонический раствор хлорида натрия (solutio Natrii chloridi isotonica 0,9 %);
• растворы новокаина (Novocainum);
• жирные растительные масла (масло персиковое — oleum Persicorum, масло миндальное — oleum Amygdalarum и др.);
• 33 % спирт этиловый (Spiritus aethylicus).
Масляные растворы нельзя вводить в вену, а спиртовые — под кожу. При назначении больших количеств жидкости, особенно при значительных кровопотерях и отравлениях, лекарственные вещества выписывают на изотоническом растворе натрия хлорида, глюкозы. Используются также коллоидные растворы для инфузий, натуральные (например, плазма нативная концентрированная) и синтетические (раствор декстрана), растворы для инфузий с содержанием комплекса электролитов (раствор Рингера-Локка) и др.
Лекарственные формы для инъекций помещают в стерильные ёмкости, изготовленные из специального стекла. Для этого используют ампулы и флаконы. После их заполнения ампулы запаивают, а флаконы герметически закупоривают. При вскрытии ампулы её содержимое теряет стерильность, поэтому эти лекарственные формы предназначены для однократного применения. Разновидностью ампул являются шприц-тюбики, которые представляют собой полиэтиленовые ампулы, соединенные с иглами. Шприц-тюбики предназначены для оказания неотложной помощи. Флаконы удобны тем, что в них можно непосредственно перед применением асептически готовить (растворять) лекарственное средство. Содержимое флакона можно использовать в несколько приёмов, сохраняя при этом стерильность препарата.
Лекарственные формы для инъекций должны быть стерильными, стойкими, апирогенными; растворы должны быть свободными от примесей и в ряде случаев изотоничными.
Концентрация раствора может обозначаться следующими способами:
1) в процентах (например, 5% — 20 ml), показывает, сколько граммов вещщества находится в 100 мл раствора;
2) в отношениях (например, 1:5000 — 400 ml). Соотношение показывает, какому количеству раствора соответствует 1,0 лекарственного вещества. 1:10 — 1,0 вещества соответствует 10 мл раствора;
3) в массо-объёмных соотношениях (например, 0,1 — 5 ml), сколько граммов вещества присутствует в конкретном взятом объёме.
Правила выписывания
Водные растворы
Водные растворы выписываются сокращенной формой прописи. После обозначения Recipe указывают название лекарственной формы в родительном падеже единственного числа с большой буквы (Solutionis), название лекарственного вещества в родительном падеже с большой буквы, концентрацию раствора и через тире его количество в мл. Второй строкой следует Da. Signa. и сигнатура. Характер раствора — водный — нигде не указывается.
Rp.: Sol. Furacilini 0,02 % — 500 ml
D.S. Для промывания раны.
Rp.: Sol. Furacilini 1:5000 — 500 ml
D.S. Для промывания раны.
Rp.: Sol. Furacilini 0,1 — 500ml
D.S. Для промывания раны.
Масляные растворы
При выписывании масляных растворов после указания лекарственной формы и названия лекарственного вещества следует обозначение — oleosae (масляного), а далее концентрация и количество раствора, Da. Signa. и сигнатура.
Rp.: Sol. Camphorae oleosae 10 % — 100 ml
D.S. Для растирания области сустава.
В том случае, когда раствор должен быть приготовлен с использованием в качестве растворителя какого-либо определенного жидкого масла, возможна лишь развернутая форма прописи.
Указывается лекарственное вещество в граммах. На второй строке — название растворителя в родительном падеже с большой буквы и его количество до нужного объёма в мл. Третья строка — Мisce. Da. Signa. (Смешай. Выдай. Обозначь.) и сигнатура.
N.B. Название лекарственной формы (раствор) не указывается.
Rp.: Anaesthesini 5,0
Olei Vaselini ad 50 ml
M.D.S. Наносить на раневую поверхность.
Спиртовые растворы
95% спиртовые растворы выписывается аналогично масляным, после указания лекарственной формы и названия лекарственного вещества следует обозначение spirituosae (спиртового), а далее концентрация и количество раствора. Следующая строка — Da. Signa. и сигнатура.
Rp.: Sol. ac. borici spirituosae 3 % — 50 ml
D.S. Для смазывания поражённых участков кожи.
В том случае, когда раствор должен быть приготовлен с использованием в качестве растворителя спирта какой-либо определенной концентрации (не 95%), возможна лишь развёрнутая форма прописи.
В названии растворителя указывается его концентрация и количество до нужного объема в мл. Название лекарственной формы (раствор) не указывается.
Rp.: Natrii tetraboratis 2,5
Spir. aethylici 9,5 % ad 10 ml
M.D.S. Наносить на раневую поверхность.
Официнальные растворы
Эти растворы выписываются без обозначения концентрации (указывается название раствора и его количество).
Rp.: Sol. Formaldehydi 200 ml
D.S. Для хирургического отделения.
Растворы для инъекций
При выписывании лекарственных форм для инъекций, которые изготавливают в аптеках (обычно растворы), обязательно указание в рецепте о стерилизации лекарства. В рецепте после обозначения лекарства отмечают — Sterilisa! или Sterilisetur! (простерилизуй! или пусть будет простерилизовано!). Если лекарство содержит несколько ингредиентов, «Sterilisetur!» ставят после «Misce». Затем следует D.S. и сигнатура.
В ампулах
Ампула представляет собой запаянный стеклянный сосуд. Ампулированные инъекционные растворы предназначаются для однократного использования. Ампулы могут иметь различную ёмкость: 1, 2, 5, 10, 50 и 100 мл. Растворы для инъекций в ампулах выписывают сокращённым способом. Ампулы обычно выписывают в количестве 5-10 шт., иногда 20-30-50 шт.
Сухое вещество в ампуле
После обозначения Recipe следует название лекарственного вещества с большой буквы в родительном падеже, его количество в одной ампуле в граммах или единицах действия. Вторая строчка — Da tales doses numero . in ampullis (Выдай такие дозы числом. в ампулах). Третья строчка — Signa. и сигнатура.
Rp.: Vincristini 0,005
D.t.d. N. 6 in amp.
S. Содержимое ампулы растворить в 5 мл воды для инъекций, вводить внутривенно 1 раз в неделю.
Rp.: Streptoliasi 250 000 ED
D.t.d. N. 6 in amp.
S. Содержимое ампулы растворить в 100 мл 5 % раствора глюкозы, вводить внутривенно капельно.
Раствор в ампуле
Выписывается как обычный раствор в сокращённой форме. Вторая строчка — Da tales doses numero . in ampullis (Выдай такие дозы числом . в ампулах). Третья строчка — Signa. и сигнатура.
Rp.: Sol. Novocaini 0,5 % — 2 ml
D.t.d. N. 6 in amp.
S. Для разведения препаратов.
Во флаконах
Ряд лекарственных веществ для инъекций выпускают в герметизированных флаконах. Объём флаконов может быть от 5 до 500 мл, а выпускают во флаконах как жидкости, так и порошкообразные вещества. Во флаконах можно ex tempore асептически готовить (растворять) лекарственные средства, а содержимое флакона можно вводить в несколько приёмов, сохраняя стерильность.
При выписывании препаратов во флаконах рецепт оформляют так же, как и в ампулах. Отличие заключается в том, что после Da tales doses numero … никаких обозначений не делают (слово «флакон» в рецепте не упоминается).
В шприц-тюбиках

Шприц-тюбик содержит стерильный раствор лекарственного вещества и предназначен для одноразового парентерального использования (под кожу, в мышцу). Шприц-тюбик состоит из полиэтиленовой ампулы и запрессованной в неё иглы, закрытой герметически колпачком. При использовании шприца-тюбика снимают колпачок, извлекают мандрен из иглы и вводят лекарственное вещество. Рецепт выписывают аналогично ампульным растворам, только необходимо указать, что следует выдать в шприц-тюбиках (D.t.d. N. in spritz-tubulis).
Rp.: Sol. Atropini sulfatis 0,1% — 1 ml
D.t.d. N. 3 in spritz-tubulis
S. По 1 мл под кожу.
Пример расчёта количества и концентрации раствора для выписывания рецепта.
Выписать раствор кальция хлорида (Calcii chloridum) на 5 дней, чтобы, применяя его внутрь по 1 столовой ложке, больной получал по 1,5 г кальция хлорида на приём. Назначить по 1 столовой ложке 4 раза в день.
1) Расчёт концентрации раствора в процентах: 1 столовая ложка = 15 мл содержит 1,5 г вещества, т. е. раствор 10%.
2) Расчёт количества раствора: 1 столовая ложка × 4 раза в день × 5 дней = 20 столовых ложек = 300 мл.
Rp.: Solutionis Calcii chloridi 10% — 300 ml
D.S. По 1 столовой ложке 4 раза в день.
В тех случаях, когда объём раствора определён, вычисляют только концентрацию.
Приготовление растворов
Растворы — однородные системы, образованные двумя или большим числом компонентов. Компонент, содержание которого в растворе преобладает, обычно называют растворителем; компонент с меньшим содержанием называют растворенным веществом.
Способы выражения концентрации растворов
Количественное содержание компонента раствора, отнесенное к определенной массе или к определенному объему раствора или растворителя, называется концентрацией этого компонента. При этом содержание растворенного вещества обычно выражают в единицах массы, в молях или в эквивалентах.
Процентная концентрация (по массе) — это число единиц массы растворенного вещества, содержащихся в 100 единицах массы раствора. (Ниже процентная концентрация обозначена С%.) Так, 20% водный раствор КОН содержит 20 единиц массы КОН и 80 единиц массы воды.
Молярная концентрация (молярность) выражается числом молей растворенного вещества в 1 л раствора и обозначается буквой М или См.
Моль — единица количества вещества. Моль — это количество вещества системы, содержащее столько молекул, атомов, ионов, электронов или других структурных единиц, сколько содержится атомов в 0,012 кг изотопа углерода 12С (6,022*10 в 23). Масса вещества, содержащаяся в 1 моле данного простого или сложного вещества, называется мольной массой. Мольная масса вещества, выраженная в граммах на моль, имеет то же численное значение, что и его относительная молекулярная масса.
Число молей простого или сложного вещества n находят из отношения массы m этого вещества в рассматриваемой системе к его мольной массе М:
Произведение объема раствора, выраженного в миллилитрах, на его молярность равно числу миллимолей растворенного вещества.
Эквивалентная концентрация (нормальность) выражается числом эквивалентов растворенного вещества в 1 л раствора и обозначается буквами N, н. или Сн.
Эквивалентом вещества называется такое его количество, которое в данной реакции равноценно (эквивалентно) 1 молю атомов водорода (1,0079 г). Масса 1 эквивалента называется эквивалентной массой.
Выражение концентрации растворов в единицах нормальности значительно упрощает вычисление объемов растворов количественно реагирующих друг с другом веществ. Эти объемы обратно пропорциональны их концентрациям, выраженным в единицах нормальности:
Произведение объема раствора, выраженного в миллилитрах, на его нормальность равно числу миллиэквивалентов растворенного вещества.
Концентрацию растворов выражают также через титр, т. е. массой (в г или мг) вещества, содержащегося в 1 мл раствора, и обозначают буквой Т. Найденную величину называют титром по растворенному (рабочему) веществу. В аналитической практике пользуются также титром по анализируемому веществу, т. е. массой (в г или мг) анализируемого вещества, эквивалентной тому количеству реагента, которое содержится в 1 мл раствора.
Например, титр 0,1 н H2SO4 (эквивалентная масса H2SO4 = 49,04 г/моль) равен:
При титровании этим раствором NaOH титр H2SO4, выраженный по анализируемому веществу NaOH (эквивалентная масса NaOH = 40,01 г/моль) равен:
Концентрацию растворов часто выражают в единицах моляльности — числом молей вещества, растворенного в 1 кг растворителя. Моляльность обозначают буквой m.
Формулы перехода от одних выражений концентрации растворов к другим
Примем следующие условные обозначения концентрации:
С% — процентная концентрация по массе;
А — число единиц массы растворенного вещества на 100 единиц массы растворителя;
Б — масса растворенного вещества в 1 л раствора;
Сн — число эквивалентов растворенного вещества в 1 л раствора (нормальность);
См — число молей растворенного вещества в 1 л раствора (молярность);
m — число молей растворенного вещества на 1000 г растворителя (моляльность);
Э — эквивалентная масса растворенного вещества, г/моль;
М — мольная масса растворенного вещества, г/моль;
d — относительная плотность.
Растворимость
Растворимость — величина, характеризующая способность вещества образовывать с данным растворителем однородную систему. Количественно растворимость газа, жидкости или твердого тела в жидком растворителе измеряется концентрацией насыщенного раствора при данной температуре.
Обычно растворимость твердых и жидких веществ выражают коэффициентом растворимости, т. е. массой вещества, растворяющегося при данных условиях в 100 единицах массы растворителя с образованием насыщенного раствора. (Насыщенным называется раствор, находящийся в равновесии с избытком растворяемого вещества.)
Каждой температуре соответствует определенная растворимость данного вещества в данном растворителе. Сведения о растворимости приводятся в справочниках.
Растворимость газов в жидкостях повышается с увеличением давления и, в большинстве случаев, с понижением температуры.
Растворимость жидких веществ в жидкостях может быть неограниченной, когда жидкие компоненты смешиваются друг с другом в любых отношениях (этиловый спирт — вода) и ограниченной в случае несмешивающихся жидкостей. В последнем случае расслаивание жидких компонентов системы зависит от температуры; обычно взаимная растворимость компонентов возрастает с температурой. Выше некоторой температурной точки, называемой критической точкой растворимости, взаимная растворимость компонентов системы становится неограниченной (расслаивания нет).
Растворимость твердых веществ в жидкостях может изменяться в широких пределах. Обычно она возрастает с повышением температуры. Однако некоторые вещества не подчиняются этому правилу: растворимость их или понижается с повышением температуры, или повышается только до некоторого предела, выше которого растворимость уменьшается.
Техника приготовления растворов
По точности выражения концентрации растворы делят на приблизительные, точные и эмпирические.
Растворы кислот и оснований приблизительной концентрации служат в качестве вспомогательных реагентов при выполнении аналитических, препаративных и других работ. Концентрацию подобных растворов рассчитывают либо по степени разбавления исходных веществ (растворов), либо по массе вещества (взвешивается на технических весах), растворенного в известной массе растворителя. Часто приблизительную концентрацию растворов определяют по величине плотности.
Растворы с точной, заранее установленной концентрацией, называемые рабочими, стандартными или титрованными растворами, служат для определения точной концентрации других растворов.
Концентрации многих растворов вспомогательных веществ (индикаторы, специфические реактивы и др.) устанавливаются эмпирически и приводятся в соответствующих прописях.
Независимо от того, какие по точности концентрации приготовляют растворы, применять следует только чистые исходные вещества и воду высокой степени очистки, а в ряде случаев (для растворов NaOH, Na2S2O3) — очищенную от CO2.
Следует иметь в виду, что скорость растворения твердого вещества зависит от размера его частиц (тонкоизмельченное растворяется быстрее).
Некоторые вещества не смачиваются водой и плавают на ее поверхности, образуя тонкую пленку. Для приготовления водных растворов подобных веществ рекомендуют порошок вначале облить небольшим количеством этилового спирта (если он инертен по отношению к компонентам раствора), а уже затем приливать воду.
Сосуды для растворения и хранения растворов оснований должны быть снабжены хлоркальциевыми трубками, заполненными аскаритом или натронной известью, чтобы защитить раствор от СO2. В некоторых случаях растворы следует хранить в атмосфере инертного газа (N2, СO2). Растворы веществ, разлагающихся под действием света, например AgNO3, следует хранить в сосудах из коричневого стекла или покрытых черным лаком (в крайнем случае обернутых в черную бумагу).
Приготовление водных растворов кислот приблизительной концентрации
Водные растворы кислот (H2SO4, HCl, HNO3) обычно приготовляют соответствующим разбавлением исходных химически чистых концентрированных кислот. Разбавление проводят из расчета на объем, так как жидкость всегда легче отмерить, чем взвесить. Чтобы получить разбавленную кислоту (например, 1:5), к 5 объемам воды прибавляют 1 объем кислоты.
Процентное содержание концентрированных кислот контролируют по плотности, определяемой большей частью ареометром. Значения концентрации кислот в зависимости от плотности см. в справочниках.
Обращаться с концентрированными кислотами следует осторожно, так как они сильно действуют на кожу, разрушают одежду и обувь, портят полы и столы. При работе с концентрированными кислотами необходимо пользоваться резиновыми перчатками и защитными очками.
При приготовлении разбавленных растворов кислот (в особенности H2SO4) следует приливать кислоту в воду тонкой струей при непрерывном перемешивании стеклянной палочкой. Если при этом смесь сильно разогрелась, то ее охлаждают, после чего приливают следующую порцию кислоты.
Кислоту, попавшую на обувь или одежду, необходимо незамедлительно смыть большим объемом воды, нейтрализовать аммиаком или NaHCO3 и снова обмыть водой. Кислоту, разлитую на столе или на полу, засыпают песком, нейтрализуют Na2CO3, СаО, Са(ОН)2, СаСО3 и лишь после этого производят уборку.
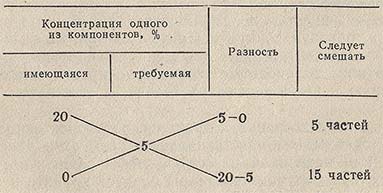
При приготовлении разбавленных растворов из более концентрированных или путем смешения растворов разных концентраций, для расчета соотношения объемов удобно пользоваться так называемым правилом креста или смешения. Это правило может быть иллюстрировано схемой получения 5% (по массе) раствора разбавлением 20% раствора:
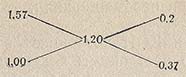
Правило креста распространяется и на случай, когда концентрация смешиваемых водных растворов выражена через плотность. Пусть дан водный раствор плотностью 1,57 г/см3. Нужно из него приготовить раствор с плотностью 1,20 г/см3. По правилу креста составляем схему:
отсюда следует, что нужно смешать 20 см3 раствора с р = 1,57 г/см3 с 37 частями по массе воды.
Расчет концентрации по правилу креста не отличается точностью, и пользоваться этим методом можно лишь для приготовления растворов приблизительной концентрации.
Приготовление безводного раствора хлорной кислоты
Раствор хлорной кислоты в безводной уксусной кислоте широко применяют в качестве титранта для кислотно-основного титрования в неводной среде.
Промышленность выпускает хлорную кислоту различной концентрации (от 42 до 70%), чаще всего в виде 57% водного раствора с плотностью около 1,50.
Избыточную воду из хлорной кислоты удаляют уксусным ангидридом:
Предварительно определив содержание воды в хлорной кислоте, последнюю растворяют в ледяной уксусной кислоте и рассчитывают, какой объем V1 (в мл) уксусного ангидрида необходим для удаления из хлорной кислоты избыточной воды:
где 100 — А — содержание воды в исходном растворе НСlO4, %; V — объем НСlO4, взятый для приготовления раствора, мл; р — плотность применяемого раствора HClO4, г/см3; p1 — плотность уксусного ангидрида, г/см3; 102 — молекулярная масса уксусного ангидрида; 18 — молекулярная масса воды.
Определенный объем HClO4 V постепенно, при непрерывном перемешивании, вливают в 800 мл ледяной уксусной кислоты, прибавляют V1 мл уксусного ангидрида, тщательно перемешивают, доводят объем раствора ледяной уксусной кислотой до 1 л и снова перемешивают. Через сутки раствор готов.
Приготовление растворов щелочей
При растворении NaOH или КОН необходимо пользоваться резиновыми перчатками и защитными очками. Щелочи вызывают химический ожог кожи, разрушают одежду и обувь. Брать твердую щелочь руками запрещается.
Водные растворы NaOH и КОН. При растворении твердых NaOH и КОН в воде происходит сильное разогревание; поэтому насыщенные растворы щелочей приготовляют в термостойкой стеклянной или, лучше, в фарфоровой посуде, постепенно добавляя твердую щелочь при перемешивании, чтобы избежать местного перегрева.
На воздухе NaOH и КОН поглощают воду и СO2. Образующиеся карбонаты мало растворимы в концентрированном растворе щелочей и постепенно выпадают в осадок.
Концентрированные растворы щелочей при хранении в стеклянной посуде разрушают стекло, выщелачивая из него кремневую кислоту. Поэтому лучше хранить их в сосудах из полиэтилена.
Из концентрированных растворов получают разбавленные растворы щелочей, концентрацию которых контролируют по плотности. Ориентировочное значение объемов разбавляемого раствора щелочи и воды можно рассчитать и по правилу креста.
Приготовление 50% раствора NaOH, не содержащего карбонатов (по ГОСТ 4517-75), производят следующим образом: в фарфоровом стакане растворяют при постепенном добавлении и перемешивании 250 г NaOH в 250 мл дистиллированной воды. После охлаждения раствор переливают в полиэтиленовый сосуд, закрывают пробкой и выдерживают 2-3 недели, до полного осаждения NaCO3. Затем прозрачный раствор сифонируют стеклянной трубкой и соответственно разбавляют водой, не содержащей СO2.
Спиртовый раствор КОН. Растворимость NaOH и КОН в метиловом спирте выше, чем в этиловом. Однако поскольку метиловый спирт очень токсичен и огнеопасен, обычно используют этанольные растворы NaOH и КОН. Растворимость NaOH в этиловом спирте при 28 °С составляет 14,7%, а КОН — 27,9%.
Для приготовления раствора КОН применяют этиловый ректификованный спирт, предварительно очищенный от альдегидов.
Наиболее эффективен следующий способ очистки: раствор из 2 г AgNO3 в 5 мл дистиллированной воды вливают в 1200 мл этилового спирта, находящегося в склянке с притертой пробкой, и тщательно перемешивают. Отдельно растворяют 5 г КОН в 25 мл горячего этилового спирта, раствор охлаждают и вливают в спиртовой раствор AgNO3. Выпадает осадок Ag2O, которому дают осесть, фильтруют и отгоняют спирт. Этиловый спирт, очищенный этим способом, остается бесцветным несколько лет.
Спиртовой раствор КОН при хранении часто приобретает слабо-желтую окраску, вызываемую осмолением примесей. Для приготовления растворов КОН, не окрашивающихся при длительном хранении, рекомендуют спирт предварительно обработать бутилатом алюминия (5 г на 1 л спирта). Смеси дают постоять 3-4 недели при комнатной температуре, после чего спирт декантируют и растворяют в нем КОН.
Приготовление водного раствора аммиака
Поступающий в продажу водный раствор аммиака плотностью 0,901-0,907 г/см3 при 20 °С, содержит 25-27% NH3. Препарат и его разбавленные растворы вполне пригодны для выполнения большинства препаративных и вспомогательных лабораторных работ.
Для аналитических работ ГОСТ 4517-75 рекомендует приготовлять растворы из баллонного жидкого синтетического аммиака или из водного аммиака, поступающего в продажу.
Газообразный аммиак вызывает раздражение глаз и слизистой оболочки носа, тошноту и головные боли. Все работы с аммиаком должны проводиться в вытяжном шкафу.
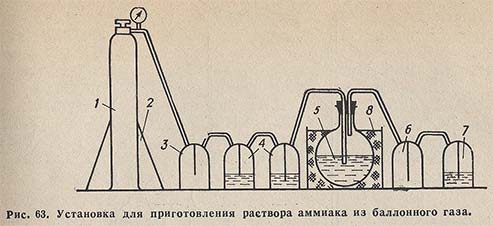
Из баллонного аммиака. Собирают установку (рис. 63). Баллон с аммиаком 1 устанавливают и закрепляют на подставке 2. Баллон соединяют с пустой промежуточной склянкой 3, к которой присоединены две поглотительные склянки 4 с раствором NaOH для поглощения СO2. Аммиак, очищенный от СO2, поступает в приемник 5, где находится дважды перегнанная дистиллированная вода, не содержащая СO2. Насыщение аммиаком проводят до достижения плотности раствора в приемнике 0,907 г/см3, что соответствует 25% раствору аммиака.
Для получения более концентрированного раствора приемник охлаждают водой со льдом в бане 8.
Склянка 6 — брызгоуловитель; склянка 7, содержащая раствор NaOH, предохраняет от попадания СO2 из воздуха в приемник.
Из водного аммиака. 500 мл водного аммиака помещают в круглодонную колбу вместимостью 1 л и осторожно прибавляют свежеприготовленную кашицу из 10 г СаО и воды.
Колбу соединяют с вертикально поставленным обратным холодильником, верхний конец которого закрывают трубкой с натронной известью, и оставляют раствор в покое на 18-20 ч. Затем собирают установку (рис. 64). Колбу 2 с водным аммиаком ставят на водяную баню 1 так, чтобы холодильник был направлен вверх под углом 45°, и соединяют верхний его конец через промежуточную колбу 4 с приемником — колбой 5, содержащей 300-400 мл воды, и закрытой трубкой с натронной известью 6. При нагревании водного аммиака на водяной бане газообразный аммиак поступает в приемник и полностью поглощается водой. Насыщение аммиаком проводят до достижения плотности раствора в приемнике 0,907 г/см3, что соответствует 25% раствору аммиака.
Приготовление рабочих растворов точной концентрации
Приготовление раствора из навески стандартного вещества. Взятую с точностью до 0,0002 г навеску высушенного стандартного вещества, которая приблизительно соответствует рассчитанной для получения определенного объема раствора заданной концентрации, аккуратно переносят в мерную колбу и растворяют в небольшом объеме дистиллированной воды, не содержащей СO2. Полученный раствор при периодическом взбалтывании разбавляют водой, доводя объем раствора в мерной колбе несколько ниже метки. Затем колбу с раствором выдерживают 15-20 мин при 20°С и осторожно добавляют воду до метки. Колбу закрывают пробкой и содержимое взбалтывают в течение 15-30 мин.
Зная массу исходного вещества и объем раствора, вычисляют его концентрацию.
Для упрощения последующих расчетов удобно пользоваться поправкой на нормальность (или коэффициентом нормальности) К. Эта поправка представляет собой отношение нормальности приготовленного раствора к заданной нормальности раствора, выраженной целыми, десятыми или сотыми долями нормальности. Например, нормальность приготовленного раствора оказалась равной 0,1036 н., а заданная 0,1 н. В этом случае
При умножении объема пошедшего на титрование раствора на эту поправку К получают эквивалентный объем заданной концентрации (в данном случае 0,1 н.).
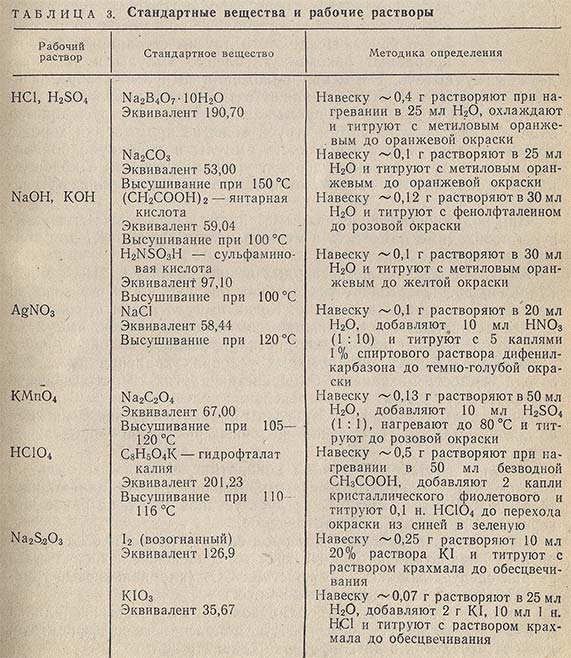
В табл. 3 приведены некоторые твердые стандартные вещества, с помощью которых точно устанавливается концентрация наиболее часто применяемых рабочих растворов.
Приготовление растворов из фиксаналов. Фиксаналы, или стандарт-титры, представляют собой точно отвешенное количество реактива или его раствора, запаянного в стеклянную ампулу. Как правило, в каждой ампуле содержится 0,1 эквивалента вещества. При количественном перенесении содержимого подобной ампулы в мерную колбу на 1 л и доведении объема раствора водой до метки при 20 °С получаются точно 0,1 н. растворы.
Выпускаются фиксаналы HCl, H2SO4, NaOH, КОН, Na2CO3, NaCl, Na2C2O4, H2C2O4-2H2O, K2Cr2O7, K2C2O4, Na2S2O3-5H2O, KMnO4, AgNO3, NH4SCN, KSCN, NaSCN, BaCl2-2H2O, (NH4)2C2O4-H2O, Na2B4O7-10H2O, KCl, K2CO3, NH4Cl, I2 и др.
Фиксаналы рекомендуется применять во всех случаях, когда требуется быстро приготовить точный рабочий раствор, не прибегая к взвешиванию.
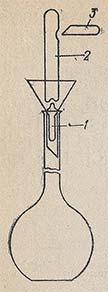
Вначале теплой водой смывают надпись на ампуле и хорошо обтирают ее чистым полотенцем. В мерную колбу вместимостью 1 л вставляют воронку с вложенным в нее стеклянным бойком (обычно прилагается к каждой коробке фиксанала), острый конец которого должен быть обращен вверх (рис. 65). Ампуле с фиксаналом дают свободно падать так, чтобы тонкое дно ампулы разбилось при ударе об острый конец бойка. После этого другим стеклянным бойком пробивают боковое углубление ампулы и дают содержимому вытечь. Не меняя положения ампулы, в образовавшееся верхнее отверстие вставляют оттянутый в капилляр и изогнутый вверх конец трубки промывалки и сильной струей промывают ампулу изнутри. Затем струей воды из промывалки хорошо промывают наружную поверхность ампулы и воронку с бойком. Удалив ампулу из воронки, доводят уровень жидкости в колбе до метки. Колбу плотно закрывают и тщательно перемешивают раствор.
При пользовании фиксаналом 0,1 н. йода перед вскрытием ампулы необходимо поместить в мерную колбу 30-40 г KI для полного растворения йода.
Ампулы с фиксаналами твердых веществ (H2C2O4-2H2O, NaCl, KMnO4 и др.) вскрывают так же, как описано выше, но воронка должна быть совершенно сухая. Когда ампула разбита, содержимое ее осторожным встряхиванием высыпают в колбу, ампулу и воронку тщательно промывают дистиллированной водой.
Фиксанал AgNO3 при обычных условиях хранения через 2-3 года темнеет. Фиксаналы большинства других твердых веществ и кислот могут храниться неопределенно долгое время.
Фиксаналы NaOH, КОН пригодны только в течение 6 месяцев со дня их выпуска. Помутнение щелочных растворов — признак их порчи.
Рабочие растворы с точной концентрацией должны быть по возможности свежеприготовленными. Исключение составляют растворы KMnO4, титр которых следует устанавливать не ранее чем через 3-4 дня после их приготовления.
При хранении рабочих растворов следует периодически проверять их концентрацию. Рабочие растворы щелочей и тиосульфата натрия следует защищать от действия СО2 (хлоркальциевые трубки с натронной известью или аскаритом).
Сосуды с рабочими растворами должны иметь четкие надписи с указанием вещества, нормальности, поправочного коэффициента, даты изготовления и даты проверки концентрации.