ПРОТИВОАРИТМИЧЕСКИЕ СРЕДСТВА
ПРОТИВОАРИТМИЧЕСКИЕ СРЕДСТВА (син. антиаритмические средства) — группа лекарственных средств, применяемых для предупреждения и купирования нарушений ритма сердечной деятельности.
Противоаритмические средства согласно классификации, предложенной в 1971—1972 гг. Сингхом и Уилльямсом (В. N. Singh, V. Е. М. Williams), делят на 4 группы.
К первой группе относят препараты, обладающие мембраностабилизирующими свойствами: хинидин (см.), новокаинамид (см.), дизопирамид (син. ритмодан), аймалин (см.), этмозин, см.), мекситил, лидокаин, тримекаин (см.) и дифенин (см.). В концентрациях, необходимых для выявления антиаритмического действия, они оказывают сопоставимое влияние на Электрофизиологические характеристики волокон миокарда. Препараты данной группы обладают способностью уменьшать максимальную скорость деполяризации клеток миокарда за счет нарушения функций так наз. быстрых натриевых каналов клеточной мембраны. В терапевтических концентрациях это действие проявляется увеличением порога возбудимости, угнетением проводимости и увеличением эффективного рефрактерного периода. При этом не происходит значительного изменения потенциала покоя мембраны клетки и продолжительности потенциала действия, но постоянно регистрируется подавление спонтанной диастолической деполяризации клеток проводящей системы сердца.
Терапевтический эффект Противоаритмических средств данной группы наблюдается при аритмиях (см. Аритмии сердца), возникающих как следствие циркуляции волны возбуждения по замкнутому КРУГУ в результате изменения эффективного рефрактерного периода, а при аритмиях, в основе которых лежит механизм усиления автоматизма или уменьшения порога возбудимости, — в результате подавления спонтанной диастолической деполяризации.
Вторая группа П. с. включает пропранолол (см.) и другие β-адреноблокаторы, которые оказывают анти-аритмическое действие гл. обр. за счет блокады симпатических влияний на сердце, осуществляемых через β-адренорецепторы. Блокаторы β-адренорецепторов, подавляя активность аденилатциклазы клеточных мембран, тормозят образование циклического АМФ, который является внутриклеточным передатчиком эффектов катехоламинов, участвующих в определенных условиях в генезе аритмий. Электрофизиологически действие препаратов этой группы в терапевтических дозах характеризуется угнетением четвертой фазы деполяризации. Однако значение этого феномена в механизме их антиаритмического действия пока неясно. β-Адреноблокаторы увеличивают продолжительность потенциала действия клеток миокарда.
Третья группа П. с. представлена амиодароном (кордарон) и орнидом (см.). Амиодарон умеренно угнетает симпатическую иннервацию, но не взаимодействует с β-адренорецепторами. В экспериментальных работах было показано, что амиодарон не оказывает мембраностабилизирующего действия и обладает крайне слабо выраженными свойствами, присущими первой группе П. с.
Орнид оказывает противоаритмическое действие, механизм к-рого остается неясным. Считают, что оно обусловлено угнетающим влиянием этого препарата на высвобождение норадреналина из окончаний симпатических нервов.
В четвертую группу П. с. входят ингибиторы трансмембранного транспорта ионов кальция. Наиболее активным является верапамил (см.). С помощью электрофизиологических методов исследования установлено, что он вызывает удлинение 1-й и 2-й фазы потенциала действия вследствие блокады кальциевых каналов клеточной мембраны, что сопровождается антиаритмическим действием. Об этом свидетельствуют такясе экспериментальные данные о роли нарушений медленного кальциевого тока через мембраны клеток миокарда в генезе некоторых видов аритмий. При таких аритмиях эктопический очаг появляется в результате активации ионного механизма по типу «медленного ответа», который в норме характерен для клеток синусового и предсердно-желудочкового узлов. Предполагают, что данный механизм участвует в возникновении аритмий, связанных как с циркуляцией волны возбуждения, так и с усилением автоматизма.
Т. о., антиаритмический эффект может быть получен в результате воздействия противоаритмических средств на различные электрофизиологические свойства клеток миокарда.
По эффективности при разных формах аритмий среди П. с. можно выделить преимущественно эффективные при наджелудочковых нарушениях ритма (напр., верапамил), гл. обр. при желудочковых аритмиях (лидокаин, тримекаин), при наджелудочковых и желудочковых аритмиях (аймалин, хинидин, новокаинамид, дизопирамид и др.).
При определении показаний к назначению П. с. должны учитываться форма аритмии, характер основного заболевания, условия, способствовавшие возникновению аритмии, а также характер и особенности действия препаратов.
Верапамил назначают при наджелудочковых экстрасистолах и наджелудочковых пароксизмальных тахикардиях, возникающих в результате циркуляции волны возбуждения в синоатриальной области, предсердиях, предсердно-желудочковом узле. Однако у больных с синдромом преждевременного возбуждения желудочков, при к-ром во время пароксизма тахикардии (особенно мерцания предсердий) импульсы в антероградном направлении проводятся по пучку Кента, верапамил может, улучшив проводимость, ухудшить течение аритмии.
Применение лидокаина и триме-каина ограничивается парентеральным введением этих препаратов с целью подавления желудочковых аритмий при остром инфаркте миокарда, хирургических операциях на сердце, интоксикациях сердечными гликозидами. В случае аритмий, связанных с гипокалиемией, указанные препараты малоэффективны. Лидокаин иногда оказывает также купирующий эффект при наджелудочковых тахикардиях, при которых в круг циркуляции волны возбуждения включаются дополнительные пути.
Дифенин назначают гл. обр. при желудочковых аритмиях, возникающих при интоксикациях сердечными гликозидами и гипокалиемии. Больным с выраженной сердечной недостаточностью и нарушением предсердно-желудочковой проводимости обычно назначают только лидокаин (в малых дозах) или дифенин; большинство П. с. им противопоказано.
При сердечной недостаточности без нарушения проводимости можно назначать, кроме этих препаратов, также этмозин и амиодарон.
При синдроме брадитахикардии (синдром слабости синусового узла) применение дизопирамида, хинидина, верапамила или блокаторов бета-адренорецепторов может привести к увеличению продолжительности асистолии, в связи с чем назначать их следует с осторожностью.
Особой осторожности требует выбор П. с. для больных с дополнительными путями проведения возбуждения в антероградном направлении по пучку Кента. Это объясняется тем, что отдельные препараты из числа П. с. купируют приступы аритмии, но не способны предупреждать их возникновение. Кроме того, некоторые П. с. могут способствовать возникновению тахикардии. Так, у больных с синдромом Вольффа—Паркинсона—Уайта и широкими желудочковыми комплексами во время пароксизма использование гликозидов или верапамила может привести к улучшению проводимости по пучку Кента, а при трепетании или мерцании предсердий вызвать фибрилляцию желудочков. В таких случаях для купирования приступа рекомендуется назначать лидокаин, новокаинамид, аймалин или амиодарон.
При узловой предсердно-желудочковой пароксизмальной тахикардии наиболее целесообразно применять верапамил, обзидан, амиодарон, а также сердечные гликозиды, обладающие способностью замедлять скорость проведения возбуждения в предсердно-желудочковом узле. При таких аритмиях новокаинамид и хинидин малоэффективны, т. к. они не влияют на проводимость в этом узле. Однако новокаинамид и хинидин могут быть использованы для предупреждения приступов, поскольку они подавляют экстрасистолию, являющуюся в определенных условиях пусковым фактором в возникновении пароксизма тахикардии.
Для купирования мерцательной аритмии рекомендуется внутривенное введение новокаинамида, аймалина, амиодарона; при удовлетворительной переносимости приступа внутрь назначают хинидин, дизопирамид или новокаинамид в соответствующих дозах. Верапамил и сердечные гликозиды используют лишь с целью урежения ритма желудочков.
У больных с желудочковой тахикардией наиболее эффективным для прерывания приступа является лидокаин, который при необходимости можно назначать в максимальной терапевтической дозе (до появления умеренно выраженных симптомов со стороны ц. п. с.). При отсутствии эффекта от лидокаина применяют другие препараты (с учетом противопоказаний) .
Тактика лечения П. с. определяется тяжестью течения заболевания и прогностическим значением имеющихся нарушений ритма сердца. Не вызывает сомнений необходимость с целью профилактики постоянного приема препаратов при часто повторяющихся (несколько раз в неделю) пароксизмах, частой экстрасистолии, сопровождающихся выраженными нарушениями гемодинамики и плохим’ самочувствием п обусловливающих потерю трудоспособности или угрожающих жизни. Больным с редкими приступами тахикардии (тахиаритмии) или со сравнительно частыми, но протекающими без резкого нарушения общего состояния приступами, которые легко купируются, можно рекомендовать прием П. с. лишь с целью их прерывания.
Тактика врача при лечении больных с экстрасистолиями, протекающими бессимптомно или с незначительными клин, проявлениями, определяется прогностическим значением экстрасистол. Проспективные наблюдения показали, что у практически здоровых лиц наджелудочковые или желудочковые экстрасистолы не опасны для жизни, поэтому случайное выявление у них бессимптомно протекающего нарушения сердечного ритма (без заболевания сердца) не должно служить показанием к применению П. с. Вместе с тем при хрон, ишемической болезни сердца желудочковые экстрасистолы значительно ухудшают прогноз для жизни, в связи с чем больным следует назначать препараты, оказывающие антиангинальное и антиаритмическое действие.
Имеются данные, свидетельствующие о возможности развития в некоторых случаях аритмогенного действия всех активных П. с. В связи с этим при синдроме Вольффа — Паркинсона — Уайта, желудочковой тахикардии и фибрилляции желудочков необходим индивидуальный подбор П. с. с помощью острых лекарственных тестов (внутривенное или пероральное введение П. с. начиная с небольших доз, которые доводят до максимально допустимых) под тщательным электрокардиографическим контролем в покое и при физической нагрузке или на фоне искусственно навязанного ритма сердца, что позволяет своевременно выявить аритмогенное действие П. с. и при необходимости оказать экстренную помощь.
При отсутствии эффекта от назначения какого-либо одного препарата используют комбинации П. с. из различных групп. Наиболее рациональным является одновременное назначение бета-адреноблокаторов с хинидином или с сердечными гликозидами. Однако не рекомендуется комбинировать П. с., имеющие одинаковый механизм действия или оказывающие противоположное влияние на Электрофизиологические свойства миокарда и проводящей системы сердца.
Клинико-фармакологическая характеристика основных П. с. приведена в таблице.
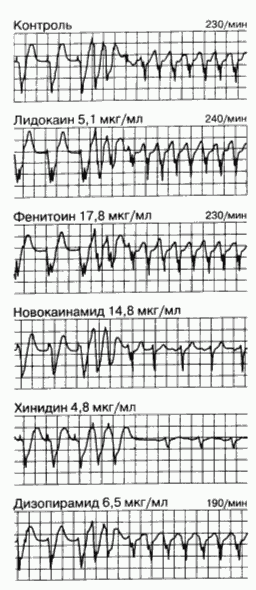 Рис. 184-10. Выбор эффективного антриаритмического препарата при желудочковой тахикардии с помощью программной стимуляции. Сверху вниз: влияние программной стимуляции без лечения (контроль) и после введения ряда антиаритмических препаратов. В контрольном исследовании нанесение двух желудочковых экстрастимулов привело к развитию желудочковой тахикардии с ритмом 230 ударов в 1 мин. Лидокаин, фенитоин и дизопирамид при указанных концентрациях в плазме не смогли предотвратить развитие тахикардии. Новокаинамид и хинидин при указанных концентрациях в плазме препятствовали возникновению стойкой тахикардии. Постоянный пероральный прием хинидина оказался эффективным методом профилактики этого нарушения ритма. (Из: J. A. Kastor et al.)
Рис. 184-10. Выбор эффективного антриаритмического препарата при желудочковой тахикардии с помощью программной стимуляции. Сверху вниз: влияние программной стимуляции без лечения (контроль) и после введения ряда антиаритмических препаратов. В контрольном исследовании нанесение двух желудочковых экстрастимулов привело к развитию желудочковой тахикардии с ритмом 230 ударов в 1 мин. Лидокаин, фенитоин и дизопирамид при указанных концентрациях в плазме не смогли предотвратить развитие тахикардии. Новокаинамид и хинидин при указанных концентрациях в плазме препятствовали возникновению стойкой тахикардии. Постоянный пероральный прием хинидина оказался эффективным методом профилактики этого нарушения ритма. (Из: J. A. Kastor et al.)